Hoy en día, la enfermedad del hígado graso no alcohólico (EHGNA) se ha convertido en la principal causa de enfermedad hepática crónica en China e incluso en el mundo. El espectro de la enfermedad incluye la esteatohepatitis hepática simple, la esteatohepatitis no alcohólica (EHNA) y la cirrosis y el cáncer de hígado relacionados. La EHNA se caracteriza por la acumulación excesiva de grasa en los hepatocitos y el daño celular e inflamación inducidos, con o sin fibrosis hepática. La gravedad de la fibrosis hepática en pacientes con EHNA está estrechamente relacionada con un mal pronóstico hepático (cirrosis y sus complicaciones, y carcinoma hepatocelular), eventos cardiovasculares, neoplasias malignas extrahepáticas y muerte por cualquier causa. La EHNA puede afectar negativamente la calidad de vida de los pacientes; sin embargo, no se han aprobado medicamentos ni terapias para su tratamiento.
Un estudio reciente (ENLIVEN) publicado en el New England Journal of Medicine (NEJM) mostró que la pegozafermina mejoró tanto la fibrosis como la inflamación hepática en pacientes con EHNA no cirróticos confirmados por biopsia.
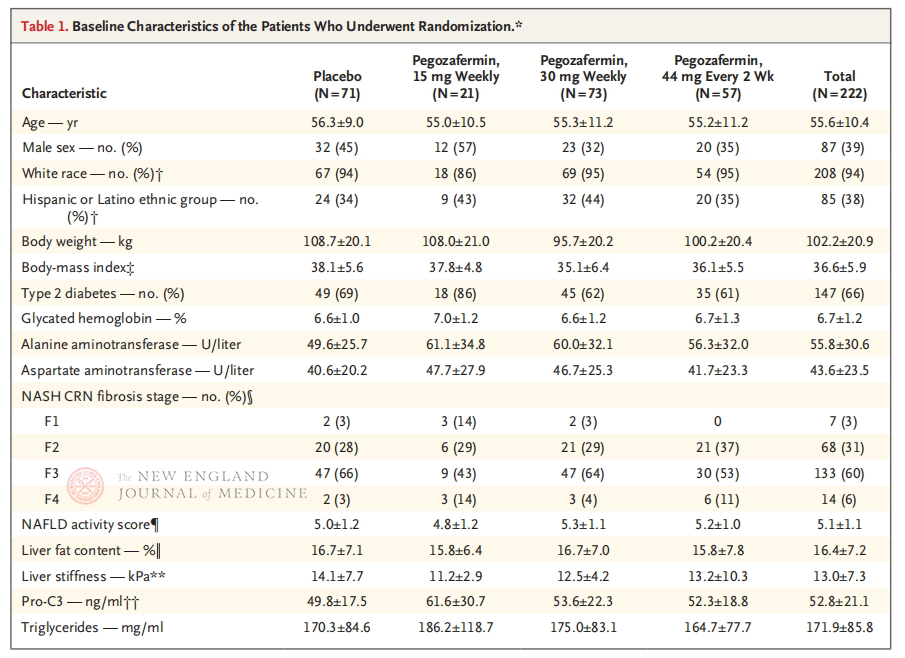
El ensayo clínico multicéntrico, aleatorizado, doble ciego y controlado con placebo de fase 2b, realizado por el profesor Rohit Loomba y su equipo clínico de la Facultad de Medicina de la Universidad de California en San Diego, incluyó a 222 pacientes con EHNA en estadio F2-3 confirmada por biopsia entre el 28 de septiembre de 2021 y el 15 de agosto de 2022. Se les asignó aleatoriamente pegozafermina (inyección subcutánea de 15 mg o 30 mg una vez a la semana, o 44 mg una vez cada 2 semanas) o placebo (una vez a la semana o una vez cada 2 semanas). Los criterios de valoración principales incluyeron una mejoría ≥ estadio 1 de la fibrosis y ausencia de progresión de la EHNA. La EHNA se resolvió sin progresión fibrótica. El estudio también realizó una evaluación de seguridad.
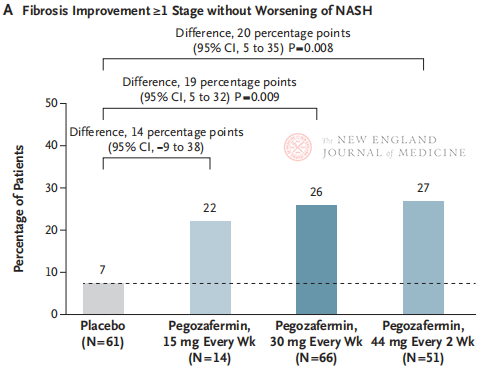
Tras 24 semanas de tratamiento, la proporción de pacientes con una mejoría ≥ estadio 1 de la fibrosis sin empeoramiento de la EHNA, así como la proporción de pacientes con regresión de la EHNA sin empeoramiento de la fibrosis, fueron significativamente mayores en los tres grupos de dosis de pegozafermina que en el grupo placebo, con diferencias más significativas en los pacientes tratados con 44 mg una vez cada dos semanas o 30 mg una vez a la semana. En términos de seguridad, la pegozafermina fue similar al placebo. Los efectos adversos más frecuentes asociados al tratamiento con pegozafermina fueron náuseas, diarrea y eritema en el lugar de la inyección. En este ensayo de fase 2b, los resultados preliminares sugieren que el tratamiento con pegozafermina mejora la fibrosis hepática.
La pegozafermina, utilizada en este estudio, es un análogo glicolado de acción prolongada del factor de crecimiento de fibroblastos humano 21 (FGF21). El FGF21 es una hormona metabólica endógena secretada por el hígado que participa en la regulación del metabolismo de lípidos y glucosa. Estudios previos han demostrado que el FGF21 tiene efectos terapéuticos en pacientes con EHNA al aumentar la sensibilidad hepática a la insulina, estimular la oxidación de ácidos grasos e inhibir la lipogénesis. Sin embargo, la corta vida media del FGF21 natural (aproximadamente 2 horas) limita su uso en el tratamiento clínico de la EHNA. La pegozafermina utiliza tecnología de pegilación glicosilada para prolongar la vida media del FGF21 natural y optimizar su actividad biológica.
Además de los resultados positivos de este ensayo clínico de fase 2b, otro estudio reciente publicado en Nature Medicine (ENTRIGUE) mostró que la pegozafermina también redujo significativamente los triglicéridos, el colesterol no HDL, la apolipoproteína B y la esteatosis hepática en pacientes con hipertrigliceridemia grave, lo que puede tener un impacto positivo en la reducción del riesgo de eventos cardiovasculares en pacientes con NASH.
Estos estudios sugieren que la pegozafermina, como hormona metabólica endógena, puede proporcionar múltiples beneficios metabólicos a los pacientes con EHNA, especialmente porque en el futuro podría denominarse enfermedad del hígado graso metabólico. Estos resultados la convierten en un fármaco potencial muy importante para el tratamiento de la EHNA. Al mismo tiempo, estos resultados positivos respaldarán la inclusión de la pegozafermina en ensayos clínicos de fase 3.
Aunque tanto el tratamiento con pegozafermina de 44 mg quincenal como el de 30 mg semanal alcanzaron el criterio de valoración principal histológico del ensayo, la duración del tratamiento en este estudio fue de tan solo 24 semanas, y la tasa de cumplimiento en el grupo placebo fue de tan solo el 7 %, significativamente inferior a los resultados de estudios clínicos previos de 48 semanas de duración. ¿Son las diferencias y la seguridad las mismas? Dada la heterogeneidad de la EHNA, se necesitan en el futuro ensayos clínicos internacionales multicéntricos de mayor tamaño para incluir poblaciones más amplias de pacientes y ampliar la duración del tratamiento para evaluar mejor la eficacia y la seguridad del fármaco.
Hora de publicación: 16 de septiembre de 2023