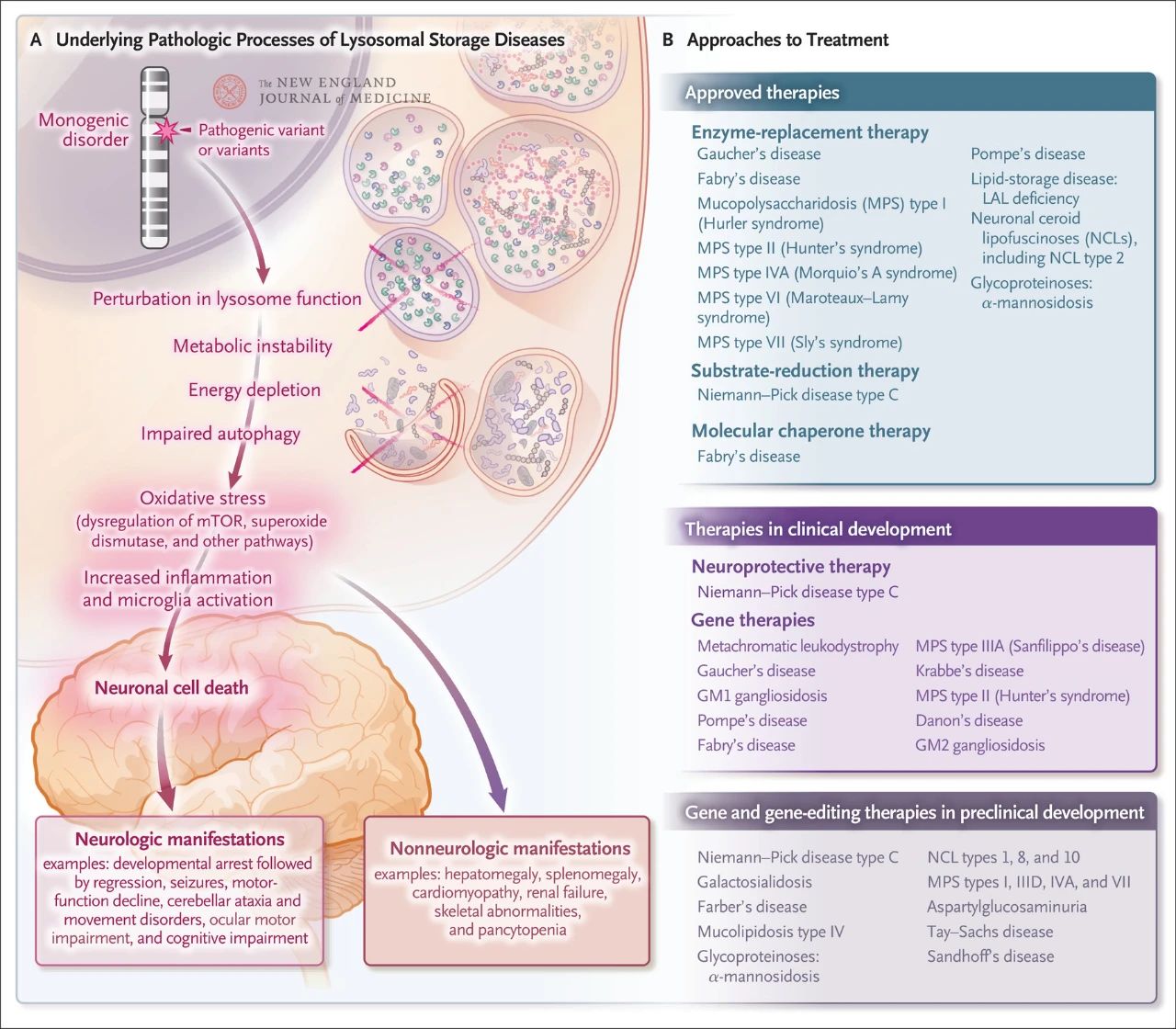
Aunque es relativamente poco frecuente, la incidencia general del almacenamiento lisosomal es de aproximadamente 1 por cada 5000 nacidos vivos. Además, de los casi 70 trastornos de almacenamiento lisosomal conocidos, el 70 % afecta al sistema nervioso central. Estos trastornos monogénicos causan disfunción lisosomal, lo que resulta en inestabilidad metabólica, desregulación de la proteína diana de la rapamicina en mamíferos (mTOR, que normalmente inhibe la inflamación), alteración de la autofagia y muerte de células nerviosas. Se han aprobado o se encuentran en desarrollo varias terapias dirigidas a los mecanismos patológicos subyacentes de la enfermedad de almacenamiento lisosomal, entre ellas la terapia de reemplazo enzimático, la terapia de reducción de sustratos, la terapia con chaperonas moleculares, la terapia génica, la edición génica y la terapia neuroprotectora.
La enfermedad de Niemann-Pick tipo C es un trastorno del transporte de colesterol en las células de almacenamiento lisosomal causado por mutaciones bialélicas en NPC1 (95%) o NPC2 (5%). Los síntomas de la enfermedad de Niemann-Pick tipo C incluyen un deterioro neurológico rápido y mortal en la infancia, mientras que las formas de inicio juvenil tardío, juvenil y adulto incluyen esplenomegalia, parálisis supranuclear de la mirada, ataxia cerebelosa, disarticulación y demencia progresiva.
En este número de la revista, Bremova-Ertl et al. presentan los resultados de un ensayo clínico cruzado, doble ciego y controlado con placebo. El ensayo utilizó un posible agente neuroprotector, el análogo del aminoácido N-acetil-L-leucina (NALL), para tratar la enfermedad de Niemann-Pick tipo C. Reclutaron a 60 pacientes adolescentes y adultos sintomáticos y los resultados mostraron una mejora significativa en la puntuación total (criterio de valoración principal) de la Escala de Evaluación y Calificación de la Ataxia.
Los ensayos clínicos de N-acetil-DL-leucina (Tanganil), un racémico de NALL y n-acetil-D-leucina, parecen basarse principalmente en la experiencia: su mecanismo de acción no se ha dilucidado con claridad. La N-acetil-DL-leucina está aprobada para el tratamiento del vértigo agudo desde la década de 1950; los modelos animales sugieren que el fármaco actúa reequilibrando la sobrepolarización y la despolarización de las neuronas vestibulares mediales. Posteriormente, Strupp et al. publicaron los resultados de un estudio a corto plazo en el que observaron mejoras sintomáticas en 13 pacientes con ataxia cerebelosa degenerativa de diversas etiologías, hallazgos que reavivaron el interés por estudiar de nuevo el fármaco.
El mecanismo por el cual la n-acetil-DL-leucina mejora la función nerviosa aún no está claro, pero los hallazgos en dos modelos murinos, uno de enfermedad de Niemann-Pick tipo C y el otro de trastorno de almacenamiento de gangliósidos GM2 variante O (enfermedad de Sandhoff), otra enfermedad lisosomal neurodegenerativa, han hecho que se preste atención a la NALL. Específicamente, la supervivencia de los ratones Npc1-/- tratados con n-acetil-DL-leucina o NALL (enantiómeros L) mejoró, mientras que la supervivencia de los ratones tratados con n-acetil-D-leucina (enantiómeros D) no lo hizo, lo que sugiere que la NALL es la forma activa del fármaco. En un estudio similar de la variante O del trastorno de almacenamiento de gangliósidos GM2 (Hexb-/-), la n-acetil-DL-leucina resultó en una extensión modesta pero significativa de la esperanza de vida en ratones.
Para explorar el mecanismo de acción de la n-acetil-DL-leucina, los investigadores investigaron la vía metabólica de la leucina midiendo metabolitos en los tejidos cerebelosos de los animales mutantes. En un modelo variante O del trastorno de almacenamiento de gangliósidos GM2, la n-acetil-DL-leucina normaliza el metabolismo de la glucosa y el glutamato, aumenta la autofagia y aumenta los niveles de superóxido dismutasa (un depurador activo de oxígeno). En el modelo C de la enfermedad de Niemann-Pick, se observaron cambios en el metabolismo de la glucosa y los antioxidantes, así como mejoras en el metabolismo energético mitocondrial. Aunque la L-leucina es un potente activador de mTOR, no se observaron cambios en el nivel ni en la fosforilación de mTOR tras el tratamiento con n-acetil-DL-leucina o sus enantiómeros en ninguno de los modelos murinos.
El efecto neuroprotector de la NALL se ha observado en un modelo murino de lesión cerebral inducida por pinzamiento cortical. Estos efectos incluyen la disminución de los marcadores neuroinflamatorios, la reducción de la muerte celular cortical y la mejora del flujo de autofagia. Tras el tratamiento con NALL, se restauraron las funciones motoras y cognitivas de los ratones lesionados y se redujo el tamaño de la lesión.
La respuesta inflamatoria del sistema nervioso central es el sello distintivo de la mayoría de los trastornos neurodegenerativos de depósito lisosomal. Si la neuroinflamación se puede reducir con el tratamiento de la LLAN, los síntomas clínicos de muchos, si no todos, los trastornos neurodegenerativos de depósito lisosomal podrían mejorar. Como demuestra este estudio, también se espera que la LLAN tenga sinergias con otras terapias para la enfermedad de depósito lisosomal.
Muchos trastornos de almacenamiento lisosomal también se asocian con la ataxia cerebelosa. Según un estudio internacional en niños y adultos con trastornos de almacenamiento del gangliósido GM2 (enfermedad de Tay-Sachs y enfermedad de Sandhoff), la ataxia se redujo y la coordinación motora fina mejoró después del tratamiento con LLAN. Sin embargo, un gran ensayo multicéntrico, doble ciego, aleatorizado y controlado con placebo mostró que la n-acetil-DL-leucina no fue clínicamente efectiva en pacientes con ataxia cerebelosa mixta (hereditaria, no hereditaria e inexplicable). Este hallazgo sugiere que la eficacia solo puede observarse en ensayos con pacientes con ataxia cerebelosa hereditaria y en los mecanismos de acción asociados analizados. Además, dado que la LLAN reduce la neuroinflamación, que puede provocar una lesión cerebral traumática, se podrían considerar ensayos con LLAN para el tratamiento de la lesión cerebral traumática.
Hora de publicación: 02-mar-2024