La hiperlipidemia mixta se caracteriza por niveles plasmáticos elevados de lipoproteínas de baja densidad (LDL) y lipoproteínas ricas en triglicéridos, lo que conduce a un mayor riesgo de enfermedad cardiovascular aterosclerótica en esta población de pacientes.
La ANGPTL3 inhibe la lipoproteína lipasa y la endosepsiasa, así como la captación hepática de lipoproteínas ricas en triglicéridos. Los portadores de la variante inactivada de ANGPTL3 presentaron niveles más bajos de triglicéridos, colesterol LDL, colesterol HDL y colesterol no HDL, así como un menor riesgo de enfermedad cardiovascular aterosclerótica. El zodasiran es un fármaco de ARN de interferencia pequeño (ARNi) que actúa sobre la expresión de ANGPTL3 en el hígado.
La hiperlipidemia mixta se refiere a niveles elevados de colesterol unido a lipoproteínas de baja densidad (cLDL) y lipoproteínas ricas en triglicéridos. Las lipoproteínas ricas en triglicéridos (incluidos los quilomicrones, las lipoproteínas de muy baja densidad [VLDL] y el colesterol residual) desempeñan un papel importante en el desarrollo de la enfermedad aterosclerótica. No existe un tratamiento eficaz para la hiperlipidemia mixta.
Se sabe que Bates reduce los niveles de triglicéridos (TG), pero esta reducción es limitada. Al mismo tiempo, los fármacos reductores de TG, incluido Bates (como el ácido acético eicosapentaenoico, etc.), no tienen un efecto significativo sobre el riesgo de enfermedad aterosclerótica causada por niveles elevados de colesterol residual. Además, estudios previos en pacientes que ya toman estatinas han demostrado que la combinación de fármacos reductores de TG no reduce el riesgo de eventos cardiovasculares. Estos factores dificultan enormemente el tratamiento de la hiperlipidemia mixta.
ANGPTL3 (proteína similar a la angiopoyetina 3) regula el metabolismo de los lípidos y las lipoproteínas, incluyendo TG y colesterol no lipoproteico de alta densidad (HDL-C), al inhibir reversiblemente la lipoproteína lipasa, la endosepiasa y la captación hepática de lipoproteínas dependiente del receptor de lipoproteína de baja densidad (LDL). Se ha encontrado que la variante de inactivación de ANGPTL3 conduce a un aumento de la actividad de la lipoproteína lipasa y la endosepiasa, lo que a su vez conduce a niveles bajos de lipoproteínas plasmáticas en la mayoría de los casos. Estas incluyen lipoproteínas ricas en triglicéridos (es decir, quilomicrones, colesterol residual, VLDL, lipoproteína de densidad media [IDL]), LDL, lipoproteína de alta densidad (HDL), lipoproteína (a) y sus componentes de colesterol. Las personas heterocigotas que portan esta variante tienen un riesgo aproximadamente 40% reducido de enfermedad aterosclerótica, y no se ha encontrado ningún fenotipo clínico adverso. ANGPTL3 se expresa en el hígado, y las terapias de silenciamiento genético dirigidas a su ARNm, conocidas como fármacos de ARN pequeño de interferencia (siRNA), son un tratamiento híbrido prometedor para la hiperlipidemia.
El 12 de septiembre de 2024, el New England Journal of Medicine (NEJM) publicó el estudio ARCHES 2, que confirma que el fármaco ARNi zodasiran redujo significativamente los niveles de triglicéridos (TG) en pacientes con hiperlipidemia mixta [1]. ARCHES-2 es un ensayo clínico de fase 2b, doble ciego, controlado con placebo y de exploración del rango de dosis. Se inscribieron 204 pacientes con hiperlipidemia mixta (TG en ayunas: 150-499 mg/dl, c-LDL ³70 mg/dl o c-no-HDL ³100 mg/dl). Se dividieron en dos grupos: zodasiran 50 mg, 100 mg, 200 mg y placebo. Los pacientes recibieron inyecciones subcutáneas en las semanas 1 y 12, y profilaxis de seguimiento hasta la semana 36.
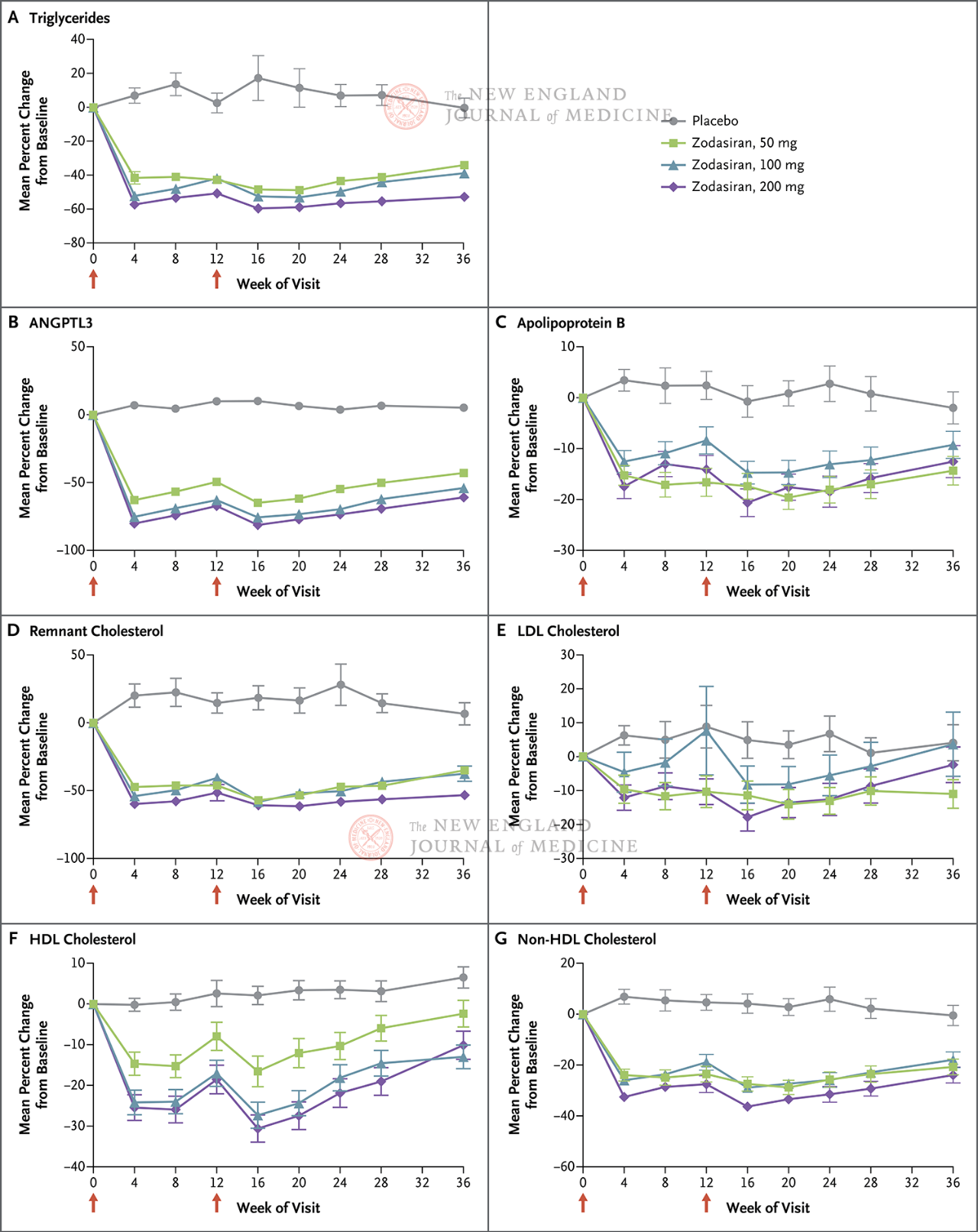
El criterio de valoración principal fue el cambio porcentual en TG desde el inicio hasta la semana 24. El estudio encontró que para la semana 24, los niveles de TG en el grupo de zodasiran se redujeron significativamente de forma dependiente de la dosis (los niveles de TG en cada grupo de dosis se redujeron en 51, 57 y 63 puntos porcentuales, respectivamente, en comparación con los del grupo placebo) (P < 0,001 para todas las comparaciones). ANGPTL3 también disminuyó en 54, 70 y 74 puntos porcentuales, respectivamente. Los niveles de colesterol no HDL disminuyeron en 29, 29 y 36 puntos porcentuales, los niveles de apolipoproteína B disminuyeron en 19, 15 y 22 puntos porcentuales, y los niveles de colesterol LDL disminuyeron en 16, 14 y 20 puntos porcentuales, respectivamente, y estos resultados persistieron hasta la semana 36. En la semana 24, zodasiran
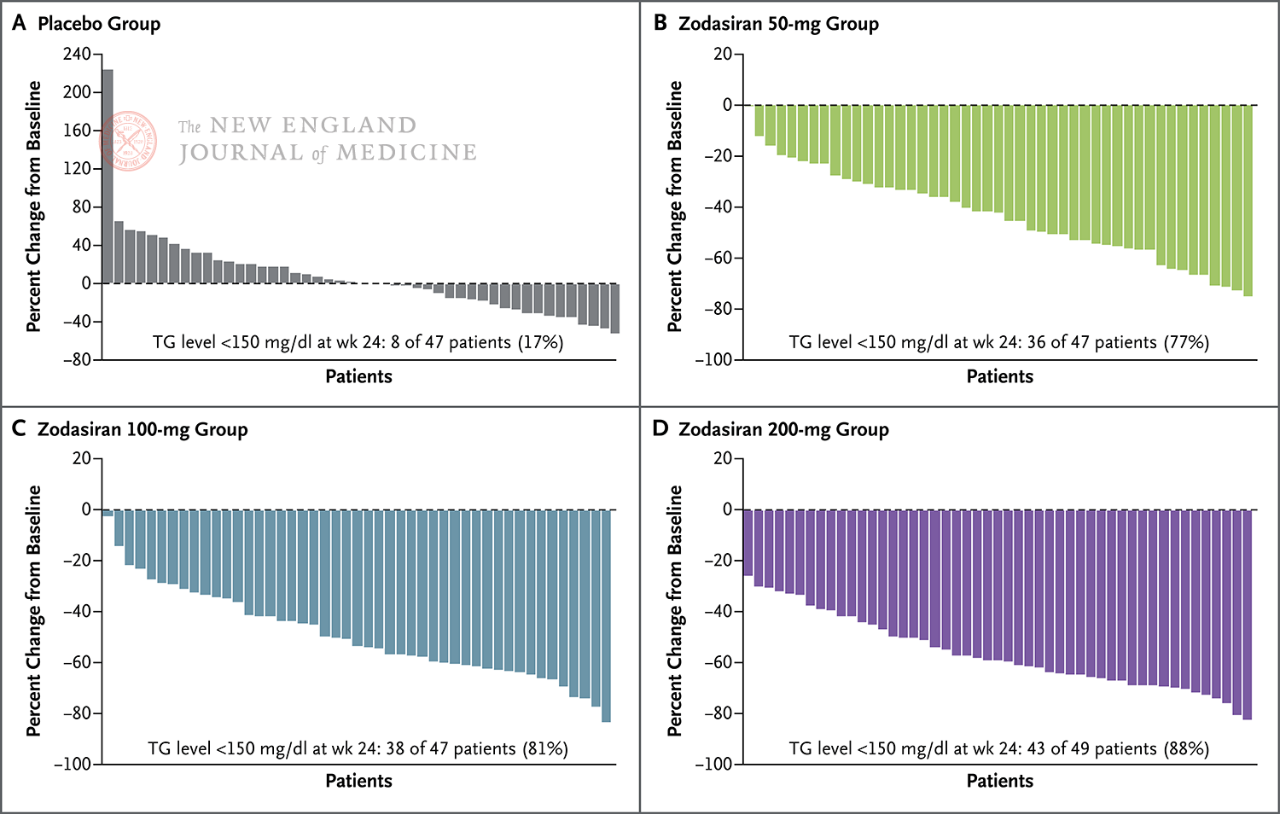
En el 88% de los pacientes del grupo de 200 mg, los TG en ayunas habían caído al rango normal.
Las flechas rojas en los días 1 y 12 indican la administración de zodasiran o placebo.
Los niveles de TG en ayunas disminuyeron a la normalidad en la semana 24 (150
mg/dL o menos)
Cada pilar representa un paciente.
El estudio también observó que zotasiran fue seguro en todos los grupos de dosis, con solo 2 pacientes que interrumpieron el estudio debido a eventos adversos (uno en el grupo placebo y uno en el grupo de 100 mg de zotasiran). Todos los eventos adversos graves en el grupo de zotasiran se recuperaron al final del estudio, y hubo una muerte en el grupo placebo. El único evento adverso preocupante fue un aumento de HbA1c en el grupo de 200 mg de zotasiran en comparación con placebo (cambio medio desde el inicio hasta la semana 24 [±DE]: 0,38 ± 0,66 % frente a -0,03 ± 0,88 % en pacientes con diabetes preexistente). En pacientes sin diabetes, el porcentaje fue del 0,12 ± 0,19 % frente al -0,03 ± 0,19 %.
En particular, casi todos los pacientes del estudio (96%) recibían tratamiento con estatinas (el 37% de las cuales eran estatinas a dosis altas), el 1% recibía un inhibidor de la enzima convertidora de proproteínas (iPCSK9) y el 21% recibía fibratos. Por lo tanto, la adición de zodasiran al régimen de tratamiento convencional actual logró efectos hipolipemiantes considerables, lo que proporciona un nuevo régimen para el tratamiento de la hiperlipidemia mixta en el futuro.
En la semana 24, la dosis máxima de 200 mg de zotasiran en el estudio redujo los niveles de colesterol residual en 34,4 mg/dl en comparación con placebo. Según los modelos actuales, se espera que esta reducción reduzca los eventos adversos cardíacos mayores en un 20 %. Zotasiran tiene el potencial de usarse como monoterapia para todos los componentes lipoproteicos y así reducir el riesgo de eventos cardiovasculares en los pacientes. Por lo tanto, se requieren más investigaciones para determinar el potencial de este fármaco para reducir el riesgo de enfermedad aterosclerótica.
El estudio MUIR de fase 2b, doble ciego, aleatorizado y controlado con placebo, publicado simultáneamente en el NEJM, utilizó otro fármaco de ARNi, plozasiran, para tratar la hiperlipidemia mixta [2]. El plozasiran está diseñado para reducir la expresión de APOC3, el gen que codifica la apolipoproteína C3 (APOC3), un regulador del metabolismo de los triglicéridos, en el hígado, reduciendo así los niveles de triglicéridos y colesterol residual. Las reducciones de los niveles de triglicéridos y colesterol residual observadas en el estudio fueron similares a las del estudio ARCHES-2. Por lo tanto, se especula que, en pacientes con hiperlipidemia mixta, ambos fármacos tienen efectos similares en la reducción de los niveles de lipoproteínas ricas en triglicéridos y colesterol residual.
Los resultados de los dos estudios de ARNi muestran que se trata de una clase de fármacos muy prometedora que aportará nuevas opciones para el tratamiento de la hiperlipidemia mixta y mejorará los resultados cardiovasculares en los pacientes.
Hora de publicación: 15 de septiembre de 2024